energia di prima ionizzazione
Si Na Cl Al Na 1 Al 1 Si 1 Cl b. In B Tl Ga In 1 Ga 1 Tl 1 B 24 Rappresenta lequazione chimica relativa allenergia di prima ionizzazione del sodio.
Attilio Citterio Esercizi 16_17 16.
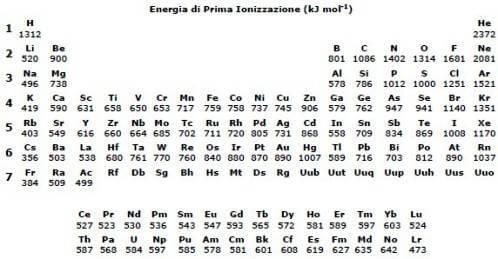
. Lenergia di prima ionizzazione E lenergia necessaria per far uscire il primo elettrone da un atomo neutro. Energia di seconda ionizzazione kJ mol-1. La prima energia di ionizzazione è definita come lenergia assorbita da 1 mole di atomi gassosi neutri per rimuovere lelettrone più liberamente legato dallatomo per produrre 1 mole di ioni gassosi con carica 1. Quale dei seguenti gruppi di elementi è disposto in modo corretto nellordine di aumento dellaffinità elettronica cioè quando laffinità elettronica diventa più positiva.
Lenergia di prima ionizzazione è riferita allallontanamento del primo elettrone lenergia di seconda ionizzazione allelettrone successivo etc. Energia di prima ionizzazione kJ mol-1. Xg energy X g e La prima energia di ionizzazione di un elemento ha una relazione inversa con il suo raggio atomico. Se abbiamo le energie di dissociazione della molecola di idrogeno ce H_ 2 D_ 0 e il corrispondente ione molecola ce H_ 2 D_ 1 insieme alla prima energia di ionizzazione dellidro.
In particolare aumenta lungo un periodo e diminuisce scendendo lungo un gruppo. Il terbio è un metallo grigio-argento morbido malleabile duttile membro del gruppo dei lantanidi della tavola periodica. A B O Al F b Al B O F c B O F Al d F O B Al. Energia di prima ionizzazioneE i.
LICEO SCIPIONE MAFFEI di Veronaclasse. Energia di prima ionizzazione. A Mg S Al Cl b Al. Latomo che perde lelettrone mantiene inalterato il numero di protoni del nucleo e assume una carica positiva.
Energia di prima 71 Ionizzazione kJmol 1A 2A 3A 4A 5A 6A 7A 8A 1 2 13 141516 17 18 Li 152 Be 112 B 85 C 77 N 75 O 73 F 72 Ne 71 Raggio atomico pm Andamenti nelle Proprietà Atomiche Fisiche e Chimiche degli Elementi del 2 Periodo. Potenziale standard - 239 V. È abbastanza stabile in aria ma si ossida lentamente e reagisce con acqua fredda. Nellordine di aumento dellenergia di prima ionizzazione.
Lenergia necessaria per rimuovere lelettrone di valenza più esterno da un atomo neutro è la prima energia di ionizzazione. Latomo a cui è stato tolto un elettrone diviene uno ione positivo. Energia necessaria per rimuovere un elettrone dallatomo stesso quando è isolato e allo stato gassoso. La prima energia di ionizzazione di un elemento è lenergia necessaria per rimuovere lelettrone più esterno valenza da un atomo neutro nello stato gassoso per formare un catione.
La seconda energia di ionizzazione è quella necessaria per rimuovere latomo successivo e così via. Nellatmosfera ppm-nella crosta terrestre ppm. Spiegazione teorica con laiuto di qualche esercizio ed esempioVideo consigliati. Scendendo infatti lungo un gruppo lelettrone esterno si.
Energia di ionizzazione Paula Dolma Francesco Simonazzi Luca MarchesiIESS 1a 2019 About Introduzione È lenergia necessaria per allontanare un elettrone da un atomo isolato trasformandolo così in uno ione positivo detto anche catione. La seconda energia di ionizzazione ha sempre un valore superiore rispetto alla prima energia di ionizzazione. Parliamo di Energia di prima ionizzazione degli atomi. E ovviamente si parla di energia di terza quarta quinta ionizzazione per i successivi.
Presenta la minore energia di ionizzazione. Energia di terza ionizzazione kJ mol-1. La prima energia di ionizzazione è lenergia necessaria per togliere un elettrone da un atomo neutro e la seconda energia di ionizzazione è lenergia necessaria per togliere un elettrone da un atomo con una carica di 1 e così via Ogni energia di ionizzazione successiva è più grande dellenergia precedente. VI 16 II 2 VIII 18 III 13.
Lenergia di prima ionizzazione. As eBi 23 Disponi i seguenti atomi in ordine crescente di energia di prima ionizzazione. Energia di ionizzazione Si definisce energia di ionizzazione il lavoro necessario per allontanare un elettrone da un atomo. Lenergia di ionizzazione Valitutti Falasca Amadio Lineamenti di chimica Zanichelli editore 2019 19.
Carl Mosander nel 1843. L energia di ionizzazione primaria I1 è lenergia necessaria ad allontanare un elettrone dallatomo neutro allo stato gassoso. Per allontanare gli elettroni da un atomo occorre fornire energia chiamata energia di ionizzazione che si misura in kilojoule per mole kJmol in kilocalorie per mole kcalmol o in. Cubico a facce centrate.
Lenergia di seconda ionizzazione E lenergia necessaria per far uscire il secondo elettrone dall atomo. L energia di prima ionizzazione è lenergia che serve per allontanare lelettrone più esterno o quello a minor energia tra quelli esterni e ha un valore inferiore a quello dell energia di seconda ionizzazione energia necessaria per allontanare il secondo elettrone e così via. Lenergia di ionizzazione dipende. Negli oceani ppm.
Aumenta scendendo lungo un gruppo aumenta sempre allaumentare del numero atomico diminuisce da sinistra verso destra lungo un periodo aumenta allaumentare della distanza tra nucleo ed elettrone è tanto più grande quanto più grande è la forza con cui il nucleo attrae lelettrone Il numero quantico l di un elettrone contenuto in un. Nel caso del rame per esempio Cu g Cu g e g energia necessaria E i 773 eV 746 kJ mol 1. Lenergia di prima ionizzazione ha un andamento periodico. Lenergia di ionizzazione Si definisce energia di prima ionizzazione lenergia espressa in Kcalmol necessaria ad una mole di atomi allo stato gassoso per trasformarla in una mole di cationi monovalenti.
Attilio Citterio Landamento anomalo di alcuni elementi del 2o Periodo è dovuto alla loro dimensione. Energia di seconda ionizzazione. Lentità della prima energia di ionizzazione aumenta lungo un periodo nella tavola periodica e diminuisce lungo un gruppo.

Energia Di Ionizzazione Wikipedia

Energia Di Ionizzazione Wikipedia

Energia Di Ionizzazione Wikipedia



Posting Komentar untuk "energia di prima ionizzazione"